微小流動,巨大洞見:微流控系統提升超分辨率顯微鏡技術
了解細胞的組織結構及其分子組分如何以協調合作的方式相互作用,是現代生命科學的核心目標。為了解答這些問題,研究人員需要同時觀察同一細胞內的多種結構,并繪制出它們的排列和相互作用圖譜。這需要“多重超分辨率顯微鏡”——一種先進的成像方法,它能夠揭示遠超傳統光學顯微鏡視野的細胞細節。
然而,現有方法往往技術要求高、難以重復,并且不太適合脆弱的生物樣本。
由哥廷根大學牽頭,并與哥廷根大學醫學中心 (UMG) 合作的國際研究團隊,作為哥廷根卓越集群“多尺度生物成像:從分子機器到可興奮細胞網絡”(MBExC) 的一部分,近期著手克服這些局限性。該團隊開發了一種專用的微流控系統,使多重超分辨率顯微鏡成像更加簡便、可重復,并能惠及更廣泛的研究群體。該研究成果發表于《ACS Nano》期刊。
為了真正了解細胞的功能,科學家不僅需要一次觀察一個細胞組分,還需要同時觀察多種蛋白質和特殊結構,并了解它們在細胞內的相互作用。此外,這些實驗變得越來越復雜,對微小的變化也越來越敏感,這會限制實驗結果的可重復性。新型微流控系統能夠精確地將溶液注入和移除樣品室,以可控且可重復的流體操作取代了手動移液。
該研究團隊開發了一種壓縮空氣驅動的微流控系統,專為多重超分辨率顯微鏡而設計,旨在為細胞(包括脆弱的生物樣本)提供便捷、經濟高效且高質量的成像。圖片來源:Roman Tsukanov
“我們開發的這套系統意味著我們可以在長時間的成像周期中保持高圖像質量,”共同第一作者、現就職于慕尼黑大學的博士后研究員薩姆拉特·巴薩克博士說。“通過保持不同標記和清洗步驟中條件的一致性,該微流控平臺能夠直接映射來自不同靶標的信息,從而實現對細胞內蛋白質、特殊結構和復雜相互作用的成像。”
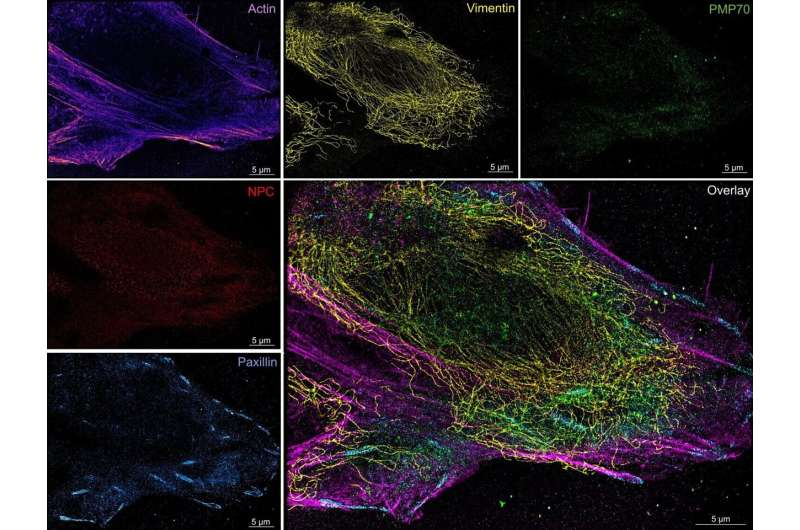
研究人員在人類癌細胞中驗證了這項技術,揭示了細胞內蛋白質絲的組織結構。該團隊還將該方法應用于從小鼠心臟心室分離出的特殊肌肉細胞。
“心臟脆弱而特殊的肌肉細胞成像難度極大,”共同第一作者、馬里蘭大學醫學中心和微流控實驗中心的Kim-Chi Vu解釋說。“微流控系統對于完成成像至關重要,它既能使細胞變形,又能防止細胞從表面脫落。”
這款新機器可以手動或自動操作,并且兼容多種成像系統。

“核心理念是開發一種經濟高效、適應性強,并且可以根據復雜生物系統的具體成像需求進行重新設計的系統,”哥廷根大學高級博士后研究員羅曼·楚卡諾夫博士解釋說。“通過自動化流體交換,我們消除了一個主要的變異來源,并使復雜的成像方案更加用戶友好。”
“這種方法將有助于標準化多重超分辨率成像,并使其得到廣泛應用,從而造福于科研和醫療應用,”哥廷根大學物理系教授 J?rg Enderlein 補充道。

